Η κιτρική τοφασιτινίμπη είναι ένα συνταγογραφούμενο φάρμακο (εμπορική ονομασία Xeljanz) που αναπτύχθηκε αρχικά από την Pfizer για μια κατηγορία από του στόματος αναστολέων κινάσης Janus (JAK). Μπορεί να αναστείλει επιλεκτικά την κινάση JAK, να μπλοκάρει τις οδούς JAK/STAT και έτσι να αναστείλει τη μεταγωγή κυτταρικού σήματος και τη σχετική γονιδιακή έκφραση και ενεργοποίηση, που χρησιμοποιείται για τη θεραπεία της ρευματοειδούς αρθρίτιδας, της ψωριασικής αρθρίτιδας, της ελκώδους κολίτιδας και άλλων ανοσοποιητικών ασθενειών.
Το φάρμακο περιλαμβάνει τρεις μορφές δοσολογίας: δισκία, δισκία παρατεταμένης αποδέσμευσης και πόσιμα διαλύματα. Τα δισκία του εγκρίθηκαν για πρώτη φορά από τον FDA το 2012 και η δοσολογική μορφή παρατεταμένης αποδέσμευσης εγκρίθηκε από τον FDA τον Φεβρουάριο του 2016. Είναι το πρώτο που θεραπεύει τις ρευματοειδή αρθρώσεις. Το Yan είναι ένας αναστολέας JAK που λαμβάνεται από το στόμα μία φορά την ημέρα. Τον Δεκέμβριο του 2019, εγκρίθηκε ξανά μια νέα ένδειξη για φάρμακα παρατεταμένης αποδέσμευσης για μέτρια έως σοβαρή ενεργό ελκώδη κολίτιδα (UC). Επιπλέον, οι τρέχουσες κλινικές δοκιμές φάσης 3 για την ψωρίαση κατά πλάκας έχουν ολοκληρωθεί και άλλες έξι κλινικές δοκιμές φάσης 3 βρίσκονται σε εξέλιξη, που περιλαμβάνουν ενεργή ψωριασική αρθρίτιδα, νεανική ιδιοπαθή αρθρίτιδα κ.λπ. Είδος ενδείξεων. Τα πλεονεκτήματα των δισκίων παρατεταμένης αποδέσμευσης που είναι μακράς δράσης και πρέπει να λαμβάνονται μόνο μία φορά την ημέρα ευνοούν τη διαχείριση και τον έλεγχο των ασθενειών των ασθενών.
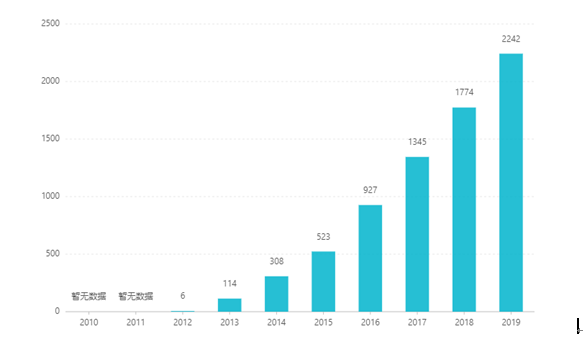
Από την εισαγωγή της στο χρηματιστήριο, οι πωλήσεις της αυξήθηκαν χρόνο με το χρόνο, φτάνοντας τα 2,242 δισεκατομμύρια δολάρια ΗΠΑ το 2019. Στην Κίνα, η δοσολογική μορφή δισκίου εγκρίθηκε για μάρκετινγκ τον Μάρτιο του 2017 και εισήλθε στον κατάλογο ιατρικής ασφάλισης κατηγορίας Β μέσω διαπραγματεύσεων το 2019. Η τελευταία νίκη η προσφορά είναι 26,79 RMB. Ωστόσο, λόγω των υψηλών τεχνικών φραγμών των παρασκευασμάτων παρατεταμένης αποδέσμευσης, αυτή η δοσολογική μορφή δεν έχει κυκλοφορήσει ακόμη στην Κίνα.
Η κινάση JAK παίζει σημαντικό ρόλο στη φλεγμονή και οι αναστολείς της έχει αποδειχθεί ότι θεραπεύουν ορισμένες φλεγμονώδεις και αυτοάνοσες ασθένειες. Μέχρι στιγμής, 7 αναστολείς JAK έχουν εγκριθεί παγκοσμίως, μεταξύ των οποίων το Delgocitinib της Leo Pharma, το Fedratinib της Celgene, το upatinib της AbbVie, το Pefitinib της Astellas, το Baritinib της Eli Lilly και το Rocotinib της Novartis. Ωστόσο, μόνο το tofacitinib, baritinib και rocotinib είναι εγκεκριμένα στην Κίνα μεταξύ των προαναφερθέντων φαρμάκων. Ανυπομονούμε να εγκριθούν το συντομότερο δυνατό τα «Tofatib Citrate Sustained Release Tablets» της Qilu και να ωφεληθούν περισσότεροι ασθενείς.
Στην Κίνα, η αρχική έρευνα για την κιτρική τοφασιτίμπη εγκρίθηκε από το NMPA τον Μάρτιο του 2017 για τη θεραπεία ενηλίκων ασθενών με ρευματοειδή αρθρίτιδα με ανεπαρκή αποτελεσματικότητα ή δυσανεξία στη μεθοτρεξάτη, με την εμπορική ονομασία Shangjie. Σύμφωνα με στοιχεία της Meinenet, οι πωλήσεις δισκίων κιτρικής τοφασιτίμπης στα δημόσια ιατρικά ιδρύματα της Κίνας το 2018 ήταν 8,34 εκατομμύρια γιουάν, που ήταν πολύ χαμηλότερες από τις παγκόσμιες πωλήσεις της. Ένα μεγάλο μέρος του λόγου είναι η τιμή. Αναφέρεται ότι η αρχική λιανική τιμή της Shangjie ήταν 2085 γιουάν (5 mg*28 δισκία) και το μηνιαίο κόστος ήταν 4170 γιουάν, κάτι που δεν είναι μικρό βάρος για τις απλές οικογένειες.
Ωστόσο, αξίζει να γιορτάσουμε ότι το tofacitib συμπεριλήφθηκε στον κατάλογο φαρμάκων «National Basic Medical Insurance, Work Injury Insurance and Maternity Insurance List» του 2019 από την Εθνική Υπηρεσία Ιατρικής Ασφάλισης μετά από διαπραγματεύσεις τον Νοέμβριο του 2019. Αναφέρεται ότι το μηνιαίο τέλος θα μειωθεί κάτω από 2.000 γιουάν μετά τη διαπραγμάτευση της μείωσης της τιμής, γεγονός που θα βελτιώσει σημαντικά τη διαθεσιμότητα του φαρμάκου.
Τον Αύγουστο του 2018, η επιτροπή επανεξέτασης διπλωμάτων ευρεσιτεχνίας του Κρατικού Γραφείου Πνευματικής Ιδιοκτησίας εξέδωσε μια απόφαση επανεξέτασης υπ' αριθ. Ωστόσο, το δίπλωμα ευρεσιτεχνίας της κρυσταλλικής μορφής Pfizertofatiib (ZL02823587.8, CN1325498C, ημερομηνία εφαρμογής 2002.11.25) θα λήξει το 2022.
Η βάση δεδομένων Insight δείχνει ότι, εκτός από την αρχική έρευνα, πέντε γενόσημα φάρμακα των Chia Tai Tianqing, Qilu, Kelun, Yangtze River και Nanjing Chia Tai Tianqing έχουν εγκριθεί για διάθεση στην αγορά στα εγχώρια σκευάσματα δισκίων tofacitinib. Ωστόσο, για τον τύπο δισκίου παρατεταμένης αποδέσμευσης, μόνο η αρχική έρευνα της Pfizer υπέβαλε αίτηση μάρκετινγκ στις 26 Μαΐου. Η Qilu είναι η πρώτη εγχώρια εταιρεία που υπέβαλε αίτηση μάρκετινγκ για αυτό το σκεύασμα. Επιπλέον, το CSPC Ouyi βρίσκεται στο δοκιμαστικό στάδιο BE.
Το Changzhou Pharmaceutical Factory (CPF) είναι ένας κορυφαίος φαρμακευτικός κατασκευαστής API, τελικών σκευασμάτων στην Κίνα, που βρίσκεται στο Changzhou, στην επαρχία Jiangsu. Τα CPF ιδρύθηκαν το 1949. Έχουμε αφιερώσει στο Tofacitinib Citrate από το 2013 και έχουμε ήδη υποβάλει DMF. Έχουμε εγγραφεί σε πολλές χώρες και θα μπορούσαμε να σας υποστηρίξουμε με την καλύτερη υποστήριξη εγγράφων για το Tofacitinib Citrate.
Ώρα δημοσίευσης: 23 Ιουλίου 2021